فرآیند مدیریت ریسک برای ایزو 13485
فرآیند مدیریت ریسک برای ایزو 13485 بخشی جدایی ناپذیر از استاندارد IEC 13485 است و تولید کنندگان را قادر می سازد .تا خطرات مرتبط با دستگاه های پزشکی خود را شناسایی، ارزیابی و کاهش دهند.
این شامل یک رویکرد سیستماتیک برای شناسایی خطرات بالقوه است که ممکن است از طراحی محصول یا فرآیندهای تولید ناشی شود.
ارزیابی احتمال وقوع این خطرات؛
ارزیابی شدت هر آسیبی که ممکن است از آنها حاصل شود.
اتخاذ اقدامات مناسب برای به حداقل رساندن یا حذف چنین خطراتی.
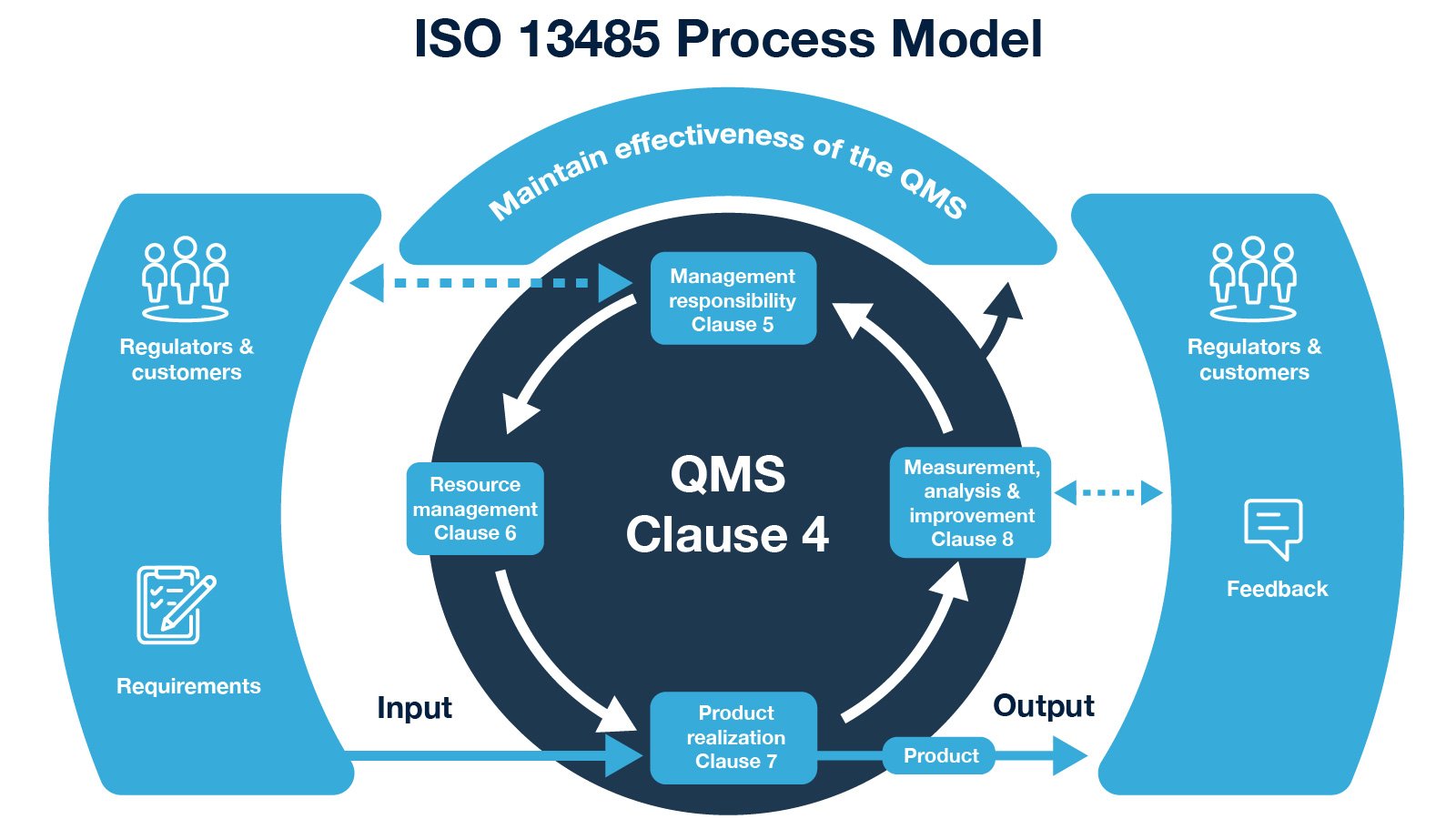
فرآیند مدیریت ریسک بخشی جدایی ناپذیر از استاندارد IEC 13485 است و تولیدکنندگان را قادر می سازد.
تا خطرات مرتبط با دستگاه های پزشکی خود را شناسایی، ارزیابی و کاهش دهند.
این شامل یک رویکرد سیستماتیک برای شناسایی خطرات بالقوه است که ممکن است از طراحی محصول یا فرآیندهای تولید ناشی شود. ارزیابی احتمال وقوع این خطرات؛ ارزیابی شدت هر آسیبی که ممکن است از آنها حاصل شود.
و اتخاذ اقدامات مناسب برای به حداقل رساندن یا حذف چنین خطراتی.
برای اطمینان از انطباق با این فرآیند، تولیدکنندگان باید تیمهای مدیریت ریسک متشکل از افرادی را ایجاد کنند .
دانش کافی در زمینه توسعه محصول و الزامات نظارتی مرتبط با دستگاههای پزشکی دارند.
علاوه بر این، باید توجه لازم را نسبت به اجرای روشهای ارتباطی مناسب بین هر یک از اعضای تیم در تمام مراحل ارزیابی ریسک ( از مفهوم اولیه تا فعالیتهای تولیدی و پس از تولید ) انجام داد.
این امر به اطمینان از دقت در هنگام محاسبه احتمالات برای خطرات احتمالی و همچنین سازگاری بین ارزیابیهای مختلف انجام شده توسط اعضای مختلف در یک تیم کمک میکند.
فایل مدیریت ریسک (RMF)
در نهایت، همه ریسکهای شناساییشده باید در یک فایل مدیریت ریسک (RMF) مستند شوند.
که باید شامل جزئیاتی مانند نوع خطر ارزیابیشده، فراوانی/احتمال پیشبینیشده وقوع، سطح شدت برآورد شده .
در صورت وقوع و اقدامات پیشنهادی کاهشدهنده به منظور کاهش اثرات آن و غیره.
RMF همچنین باید شامل بررسی های دوره ای در برابر اهداف تعیین شده برای ابتکارات بهبود باشد .
به حفظ تضمین کیفیت در طول زمان کمک می کند و در عین حال رضایت مشتری را از محصولات عرضه شده توسط سازمان شما به بازار تضمین می کند.
فرآیند مدیریت ریسک در ISO 13485
طبق الزامات ISO 13485، فرآیند مدیریت ریسک باید شامل مراحل زیر باشد:
- شناسایی ریسکها:
- این مرحله شامل شناسایی تمامی خطرات بالقوهای است که ممکن است در طول چرخه عمر محصول رخ دهند. این خطرات میتوانند شامل ریسکهای ناشی از نقص در طراحی، تولید، بستهبندی، حملونقل و استفاده باشند.
- ارزیابی ریسکها:
- پس از شناسایی خطرات، هر ریسک باید از لحاظ شدت و احتمال وقوع ارزیابی شود. این ارزیابی به شرکتها کمک میکند تا تعیین کنند کدام ریسکها به مداخلات بیشتری نیاز دارند.
- کنترل ریسکها:
- پس از ارزیابی، شرکت باید اقداماتی برای کاهش یا حذف ریسکها اجرا کند. این اقدامات میتوانند شامل تغییر در طراحی محصول، اصلاح فرآیندهای تولید یا ارائه دستورالعملهای ایمنی برای کاربران نهایی باشند.
- نظارت و ارزیابی مداوم:
- مدیریت ریسک یک فرآیند پویاست و باید بهطور مداوم در طول عمر محصول انجام شود. بهروزرسانیهای منظم در فرآیندها و محصولات میتوانند منجر به کاهش بیشتر ریسکها شوند.
ابزارهای مورد استفاده در مدیریت ریسک ISO 13485
برای اجرای مؤثر مدیریت ریسک در سیستمهای مدیریت کیفیت، از چندین ابزار و روش مختلف استفاده میشود. برخی از این ابزارها شامل موارد زیر هستند:
- FMEA (تحلیل حالتهای خرابی و اثرات آن):
- این ابزار برای شناسایی و تحلیل خرابیهای احتمالی در یک سیستم یا فرآیند مورد استفاده قرار میگیرد و به تشخیص ریسکهای مرتبط کمک میکند.
- FTA (تحلیل درخت خطا):
- این روش به شناسایی علتهای بالقوه خطا و ارزیابی تأثیرات آنها بر روی محصول کمک میکند.
- HACCP (تحلیل مخاطرات و کنترل نقاط بحرانی):
- این ابزار بهطور خاص برای صنایع غذایی و تجهیزات پزشکی کاربرد دارد و به شناسایی و کنترل ریسکها در مراحل کلیدی تولید کمک میکند.
مزایای مدیریت ریسک برای شرکتها
اجرای فرآیند مدیریت ریسک مطابق با استاندارد ISO 13485 برای شرکتهای تولیدکننده تجهیزات پزشکی مزایای بسیاری دارد:
- کاهش خطرات مرتبط با ایمنی:
- با شناسایی و کاهش ریسکهای احتمالی، شرکتها میتوانند از بروز مشکلات ایمنی در محصولات خود جلوگیری کنند.
- افزایش اعتماد مشتریان:
- اجرای سیستمهای قوی مدیریت ریسک به بهبود کیفیت محصولات و افزایش اعتماد مشتریان و مقامات نظارتی منجر میشود.
- موافقت با مقررات:
- رعایت الزامات مدیریت ریسک مطابق با ISO 13485 کمک میکند تا محصولات با قوانین و مقررات جهانی مطابقت داشته باشند و موانع قانونی را در بازارهای بینالمللی کاهش دهند.
مدیریت ریسک در ISO 13485 و گواهینامه CE
مدیریت ریسک در ISO 13485 و گواهینامه CE هر دو بهطور مستقیم با تضمین سیستم مدیریت ایمنی و بهداشت و کیفیت محصولات پزشکی مرتبط هستند.
گواهینامه CE نشاندهنده تطابق یک محصول با مقررات اتحادیه اروپا از جمله دستورالعملهای ایمنی است، و مدیریت ریسک بخش مهمی از این فرآیند است.
در واقع، برای دریافت گواهینامه CE، تولیدکنندگان تجهیزات پزشکی باید نشان دهند که ریسکهای مرتبط با طراحی و تولید محصول را بهطور کامل شناسایی، ارزیابی و کنترل کردهاند. این الزامات مشابه با استاندارد ISO 13485 است، که مدیریت ریسک را یکی از اصول اساسی سیستم مدیریت کیفیت خود قرار میدهد. بنابراین، مدیریت ریسک در ISO 13485 نه تنها به بهبود کیفیت محصول کمک میکند، بلکه پیششرطی برای دریافت گواهینامه CE نیز محسوب میشود و به شرکتها اجازه میدهد تا محصولات خود را در بازارهای اروپایی عرضه کنند.
جهت مشاوره ایزو 13485 بیشتر با کارشناسان آریان گستر تماس حاصل فرمایید .
02177942240 02177959675
جهت اطلاعات بیشتر و مشاوره برای گواهینامه ایزو با مشاوران آریان گستر تماس حاصل فرمایید. 02177942240 - 02177953675

